24 март 2026 година го одбележува 31-виот Светски ден на туберкулозата. Светската здравствена организација (СЗО) ја објави глобалната тема за оваа година како„Да! Можеме да ја искорениме туберкулозата!“, нагласувајќи дека силното владино водство, одржливата политичка посветеност и координираната мултисекторска акција се од суштинско значење за ставање крај на епидемијата на туберкулоза (ТБ).

Глобален напредок и преостанати предизвици
Според Глобалниот извештај за туберкулоза 2025 година, глобалната контрола на туберкулозата достигна значајна пресвртница во 2024 година, со двете...инциденцата и смртноста се намалуваатза прв пат од пандемијата на COVID-19.
Проценето10,7 милиони луѓеразвиле туберкулоза во 2024 година, вклучувајќи 54% мажи, 35% жени и 11% деца и адолесценти. Меѓу овие случаи, приближно619.000 (5,8%)биле коинфицирани со ХИВ, и390.000 (3,6%)беа мултирезистентни на лекови или рифампицин-резистентни на туберкулоза (MDR/RR-TB).
ТБ предизвикана приближно1,23 милиони смртни случаиво 2024 година, останувајќи водечка заразна причина за смрт на глобално ниво, надминувајќи го COVID-19. По три години зголемување помеѓу 2021 и 2023 година, глобалната инциденца на туберкулоза се намали за речиси 2% во 2024 година, што одразува постепено закрепнување на услугите за туберкулоза.[1]
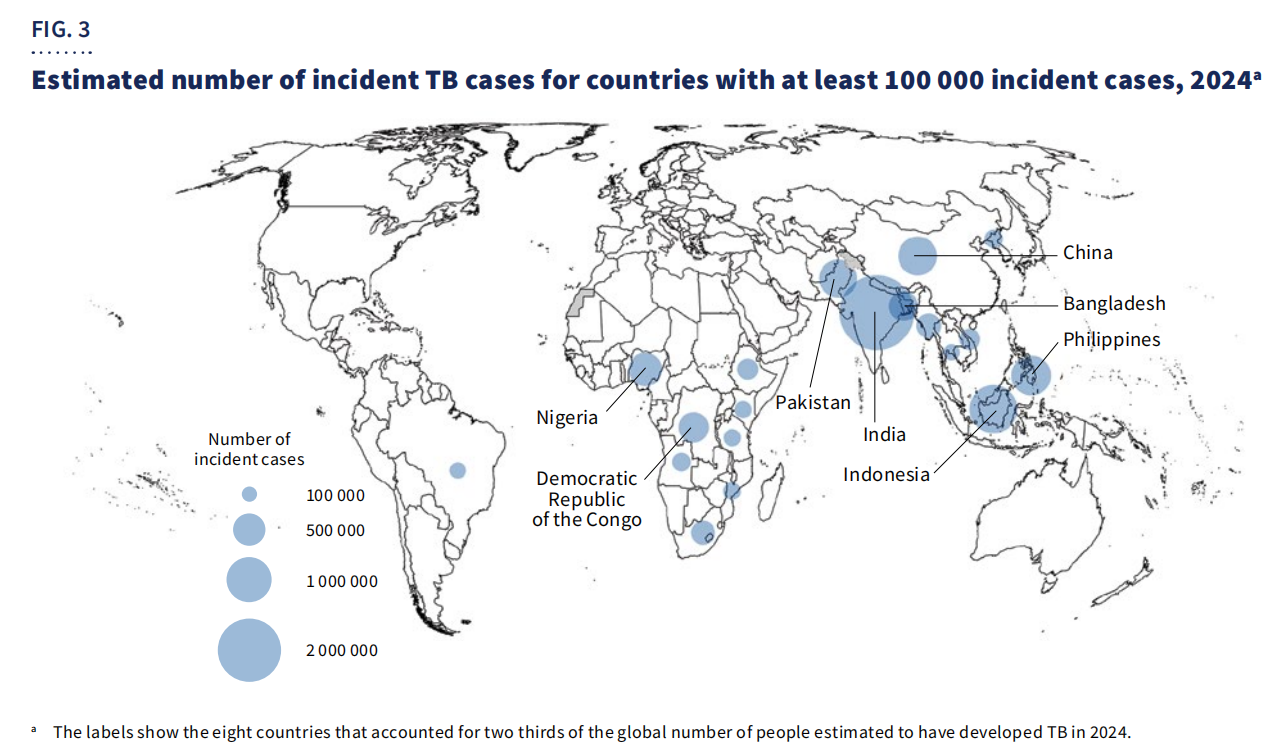
Географски,67% од случаитебеа концентрирани во осум земји: Индија, Индонезија, Филипини, Кина, Пакистан, Нигерија, Демократска Република Конго и Бангладеш.
И покрај напредокот, туберкулозата останува водечка причина за смрт кај луѓето што живеат со ХИВ и главен фактор за смртноста поврзана со антимикробната резистенција. Глобалното финансирање продолжува да биде недоволно, со само5,9 милијарди американски доларидостапни во 2024 година - далеку подГодишна цел од 22 милијарди американски доларипоставен за 2027 година.
Овие бројки ја истакнуваат итната потреба од зајакнување на програмите за контрола на туберкулозата на глобално ниво, со фокус на проширување на пристапот до дијагностика, подобрување на резултатите од третманот и справување со социјалните детерминанти кои го поттикнуваат преносот на туберкулозата. Туберкулозата продолжува да бара силна меѓународна соработка и политичка посветеност за да се исполнат целите на Стратегијата за искоренување на туберкулозата.
Микобактериум туберкулоза: Патогенеза и класификација
Mycobacterium tuberculosis (MTB/M. tuberculosis) е примарен и најчест патоген одговорен за туберкулоза (ТБ). Може да влезе во човечкото тело преку респираторниот тракт, дигестивниот тракт или оштетената кожа и мукозните мембрани, инфицирајќи повеќе органи и предизвикувајќи различни форми на ТБ. Белодробната туберкулоза, која првенствено се пренесува преку капки, сочинува повеќе од 80% од случаите на ТБ. Вообичаените симптоми вклучуваат кашлање, производство на спутум и хемоптиза. По инфекцијата во белите дробови, бактеријата може да се прошири преку крвотокот до повеќе системи, што потенцијално може да доведе до скелетна, уринарна или гастроинтестинална туберкулоза.[2]
MTB е дел од родот Mycobacterium, кој вклучува:
- Комплекс од микобактериум туберкулоза (MTBC): Содржи M. tuberculosis, M. bovis, M. africanum, M. canettii и M. microti, меѓу другите. Иако M. tuberculosis е примарна причина за туберкулоза, M. bovis и M. africanum исто така можат да ја предизвикаат болеста.
- Нетуберкулозни микобактерии (NTM).
- Mycobacterium leprae, предизвикувач на лепра.
Лабораториски дијагностички пристапи
Точната и навремена дијагноза е од суштинско значење за ефикасна контрола на туберкулозата. Светската здравствена организација нагласува декаБрзите молекуларни дијагностички технологии фундаментално го трансформираа откривањето на туберкулозата, овозможувајќи високо чувствителна и специфична идентификација на патогени, а истовремено откривајќи отпорност на лекови.[1].
- Микроскопија и култураe: Културата останува златен стандард за дијагностицирање на туберкулоза, бидејќи овозможува дефинитивна идентификација на одржливи организми и го поддржува тестирањето на осетливоста на лекови и геномската анализа. Сепак, поради бавната стапка на раст на Mycobacterium tuberculosis, резултатите обично се добиваат од 2 до 8 недели, што ја ограничува нејзината клиничка корисност при итно донесување одлуки.
-Имунолошки тестирања: Имунолошките методи, вклучувајќи го туберкулинскиот тест на кожата (TST) и тестовите за ослободување на интерферон-гама (IGRA), ги детектираат имунолошките одговори на домаќинот на инфекција со туберкулоза. Иако се корисни за идентификување на латентна инфекција, овие тестови не можат со сигурност да разликуваат помеѓу активна и претходна инфекција и затоа имаат ограничена дијагностичка специфичност во услови со висок товар.
-Молекуларна дијагностика (NAAT): Тестовите базирани на ДНК, како што е амплификацијата на нуклеинска киселина (NAAT), се препорачуваат поради нивната висока чувствителност и специфичност.
-Целно секвенционирање од следната генерација (tNGS): Технологиите за целно секвенционирање овозможуваат идентификација со висока резолуција на мутации поврзани со резистенција. Упатствата на СЗО го препорачуваат tNGS како напредна алатка за постдијагностичко откривање на резистенција на лекови, поддржувајќи ги прецизните стратегии за третман [3].
-Метагеномско секвенционирање од следната генерација (mNGS): Метагеномското секвенционирање овозможува непристрасно откривање на широк спектар на патогени без претходен избор на цел. Овој пристап е особено вреден во сложени или нејасни клинички сценарија, вклучувајќи мешани инфекции и имунокомпромитирани пациенти, каде што конвенционалната дијагностика може да биде недоволна.
СЗО дополнително нагласува дека микробиолошката потврда е од суштинско значење за започнување соодветна терапија и подобрување на исходите кај пациентите, зајакнувајќи ја важноста на интегрирањето на напредната молекуларна дијагностика во програмите за контрола на туберкулозата [1].
Сеопфатни молекуларно-дијагностички решенија од макро и микро-тест
1.Мултиплекс PCR детекција за туберкулоза и отпорност на лековиТБ
| Код на производ | Име на производ | Сертификација |
| HWTS-RT001 | Комплет за детекција на ДНК од микобактериум туберкулоза (флуоресцентна PCR) | CE |
| HWTS-RT137 | Комплет за детекција на мутации на отпорност на Mycobacterium Tuberculosis изонијазид (крива на топење) | CE |
| HWTS-RT074 | Комплет за детекција на отпорност на нуклеинска киселина и рифампицин од Mycobacterium Tuberculosis (крива на топење) | CE |
| HWTS-RT102 | Комплет за детекција на нуклеински киселини базиран на изотермна амплификација (EPIA) со ензимска сонда за Mycobacterium tuberculosis | CE |
| HWTS-RT144 | Комплет за детекција на нуклеинска киселина со лиофилизиран микобактериум туберкулоза комплекс (изотермна амплификација со ензимска сонда) | CE |
| HWTS-RT105 | Комплет за детекција на ДНК на Mycobacterium Tuberculosis, сушен со лиофилизација (флуоресцентна PCR) | CE |
| HWTS-RT147 | Комплет за детекција на нуклеинска киселина и рифампицин, изонијазид (крива на топење) | CE |
Кога постои силно клиничко сомневање за туберкулоза (ТБ),HWTS-RT147тестот се препорачува за квалитативно откривање на инфекција со MTB и туберкулоза отпорна на повеќе лекови (MDR-TB). Овој тест идентификува мутации воrpoB ген, што доведува до резистенција на рифампицин (RIF) и мутации воkatG и InhA гени, кои се поврзани со резистенција на изонијазид (INH). Обезбедува ефикасен, еднократен тест и за MTB и за MDR-TB, вклучувајќи внатрешна контрола на квалитетот за да се минимизираат лажно негативните резултати, обезбедувајќи брзи и точни резултати.
2.PTNseq таргетирано секвенционирање за респираторни патогени и профилирање на отпорност
| Код на производ | Име на производ | Спецификација |
| HWKF-TS0001 | Комплет за збогатување на гени за патогени на инфекции во крвотокот PTNseq | 24 тестови/комплет |
| HWKF-TS0002 | PTNseq комплет за збогатување на гени за инфекција на централниот нервен систем кај патогени микроорганизми | 24 тестови/комплет |
| HWKF-TS0003 | Комплет за збогатување на гени за патогени на респираторни инфекции PTNseq | 24 тестови/комплет |
| HWKF-AT0003 | PTNseq Комплет за автоматско збогатување на библиотеката за респираторна инфекција, патогени микроорганизми (ONT) | 24 тестови/комплет |
| HWKF-TS0004 | Комплет за збогатување на гени за инфективни патогени со широк спектар на PTNseq | 24 тестови/комплет |
| HWKF-TS0005 | Комплет за збогатување на гени за инфективни патогени микроорганизми со ултра-широк спектар на PTNseq | 24 тестови/комплет |
| HWKF-TS0151 | Комплет за типизација на микобактериум и збогатување на гени за отпорност на лекови (метод на повеќекратна амплификација) | 24 тестови/комплет |
Во случаи на мешани респираторни инфекции (вклучувајќи инфекции на горниот и долниот респираторен тракт, туберкулоза и хронични респираторни заболувања) или кога е потребна анализа на гените за отпорност на лекови (на пр., сомневање за туберкулоза отпорна на лекови),PTNseq серија на насочена детекција на гени со висок протокможе да се примени. Врз основа на напредна технологија за целно секвенционирање, PTNseq користи ултра-мултиплекс PCR за збогатување на специфични целни секвенци, во комбинација со секвенционирање со висок проток и технологија на нанопори од трета генерација за сеопфатна идентификација на патогени и профилирање на отпорност на лекови.
Системот користи патентирани, високоспецифични прајмери за ултра-мултиплекс амплификација на целните гени. Поддржан од сопствена база на податоци и интелигентни биоинформатички алгоритми, тој обезбедува прецизна идентификација на патогени, заедно со анализа на гени за отпорност на лекови и вируленција. Целното збогатување ги намалува пречките од ДНК-та на домаќинот, подобрувајќи ја чувствителноста кај примероците со висока човечка позадина и овозможувајќи ефикасно откривање на тешки цели како што сеМикобактериум туберкулоза, габи, интрацелуларни бактерии, РНК вируси и гени за отпорност или вирулентност.
PTNseq постигнува граница на детекцијасамо 100 копии/мли покрива175 вообичаени респираторни патогени, вклучувајќи 76 бактерии, 73 вируси, 19 габи, 7 микоплазми, како иКламидија, Рикецијаи 54 гени за отпорност на лековиПанелот ги вклучуваМикобактериум туберкулозакомплексни и големи нетуберкулозни микобактерии.
Серијата PTNseq комбинира висока чувствителност со економичност, подобрувајќи ги стапките на откривање на патогени и поддржувајќи индивидуализирана антимикробна терапија, а воедно помагајќи во ублажување на антимикробната резистенција. Интегрирана со целосно автоматизираниот систем за подготовка на библиотека за секвенционирање на гени (AIOS), таа обезбедува поедноставно, болничко решение со време на обработка од само 6,5 часа од земање на примерокот до резултатот.

3. Метагеномско секвенционирање за откривање на патогени со широк спектар
| Код на производ | Име на производ | Спецификација |
| HWKF-MN0011 | Комплет за детекција на метагеномски патогени (ДНК-Илумина) | 24 тестови/комплет |
| HWKF-MN0018 | Комплет за детекција на метагеномски патогени (ДНК-МГИ) | 24 тестови/комплет |
| HWKF-MN0021 | Комплет за детекција на метагеномски патогени (ДНК-ОНТ) | 24 тестови/комплет |
| HWKF-MN0012 | Комплет за детекција на метагеномски патогени (РНК-Илумина) | 24 тестови/комплет |
| HWKF-MN0019 | Комплет за детекција на метагеномски патогени (РНК-МГИ) | 24 тестови/комплет |
| HWKF-MN0022 | Комплет за детекција на метагеномски патогени (РНК-ОНТ) | 24 тестови/комплет |
| HWKF-MN0013 | Комплет за детекција на метагеномски патогени (ДНК+РНК-Илумина) | 24 тестови/комплет |
| HWKF-AYM0013 | КиТ за автоматска конструкција на библиотека за детекција на метагеномски патогени (ДНК+РНК-Илумина) | 24 тестови/комплет |
| HWKF-MN0020 | Комплет за детекција на метагеномски патогени (ДНК+РНК-МГИ) | 24 тестови/комплет |
| HWKF-MN0023 | Кит за откривање на метагеномски патогени (ДНК+РНК-ОНТ) | 24 тестови/комплет |
Кога клиничката дијагноза е нејасна,Детекција на гени со висок проток на патогени на mNGSможе да се изврши на различни примероци од пациентот, вклучувајќи течност од бронхоалвеоларна лаважа, спутум, брисеви од грло, крв, плеврален излив, гној и примероци од ткиво. Овој пристап користи технологија на метагеномско секвенционирање, каде што различни примероци се подложени на целен претходен третман проследен со екстракција на нуклеинска киселина со употреба на стаклени зрна и ензими за варење на ѕидовите, со што се подобрува ефикасноста на екстракцијата. Секвенционирањето е прилагодено на повеќе платформи, обезбедувајќи голем обем на податоци за подобрена чувствителност на mNGS и интегритет на склопувањето. Податоците се анализираат со помош на самоизградена база на податоци и интелигентни алгоритми за откривањенад 20.000 патогени, вклучувајќи бактерии, габи, вируси и паразити, давајќи информации за сомнителни патогени микроорганизми. Овој метод е погоден за пациенти со тешка дијагноза, критично болни или имунокомпромитирани пациенти, вклучувајќи идентификација наМТБкомплексениНТМ, како и мешани инфекции. Значително ги подобрува стапките на откривање на патогени и помага во насочувањето на клиничката целна употреба на антибиотици, овозможувајќи прецизна дијагноза на инфекции.
Заклучок
Иако е постигнат значителен напредок, туберкулозата останува голем глобален здравствен предизвик, особено во контекст на отпорност на лекови, недостатоци во финансирањето и нееднаков пристап до дијагностика.
СЗО нагласува дека зголемувањето на пристапот до брза молекуларна дијагностика и напредни технологии за секвенционирање е од суштинско значење за постигнување на целите на Стратегијата за искоренување на туберкулозата. Со континуирани иновации, инвестиции и глобална соработка, искоренувањето на туберкулозата повеќе не е аспирација, туку остварлива цел.
Референци:
- Светска здравствена организација. Глобален извештај за туберкулоза 2024/2025: Дијагностичко тестирање и третман.
- Светска здравствена организација. Прирачник на СЗО за избор на молекуларни брзи дијагностички тестови препорачани од СЗО за откривање на туберкулоза и туберкулоза отпорна на лекови.
- Светска здравствена организација. Консолидирани упатства на СЗО за туберкулоза: Модул 3 – Дијагноза (ажурирање од 2024 година).
Време на објавување: 24 март 2026 година
